21调查|医美乱象频现!5万元美容针竟是“骨科材料”
21世纪经济报道记者韩利明
日前,杭州电视台官微发布一篇名为《杭州思达芮医疗数万元打的美容针竟是“骨科材料”疑似违规用药》的报道,再度将羟基磷灰石(CaHA)这一医美新材料的使用乱象推向公众视野。
报道披露,今年8月,市民骆女士在杭州思达芮医疗美容诊所花费50830元,注射了宣称可以刺激胶原蛋白再生、让皮肤变得更有弹性的“菲林普利”,然而事后发现该产品不具备面部医美注射的资质。
骆女士同时反映,该诊所仅告知产品功效,未详细说明注射部位及次数,且事后核对发现,诊所收取了鼻基底1针的费用,但她并未接受该部位注射。无独有偶,另一位投诉人章女士也反映,其在该诊所注射“菲林普利”时,遭遇了与骆女士一样的“未注射却收费”问题。
公开信息显示,菲林普利是成都睿合医药旗下的医美品牌,产品由四川拜阿蒙生物材料公司研发生产。国家药监局官网信息明确其注册全称为“羟基磷灰石生物陶瓷”,适应范围为“各种原因所致的骨缺损修复或填充;各种原因所致的软组织修复或增强,如眼球摘除或眼内容物剜除后的义眼台植入”。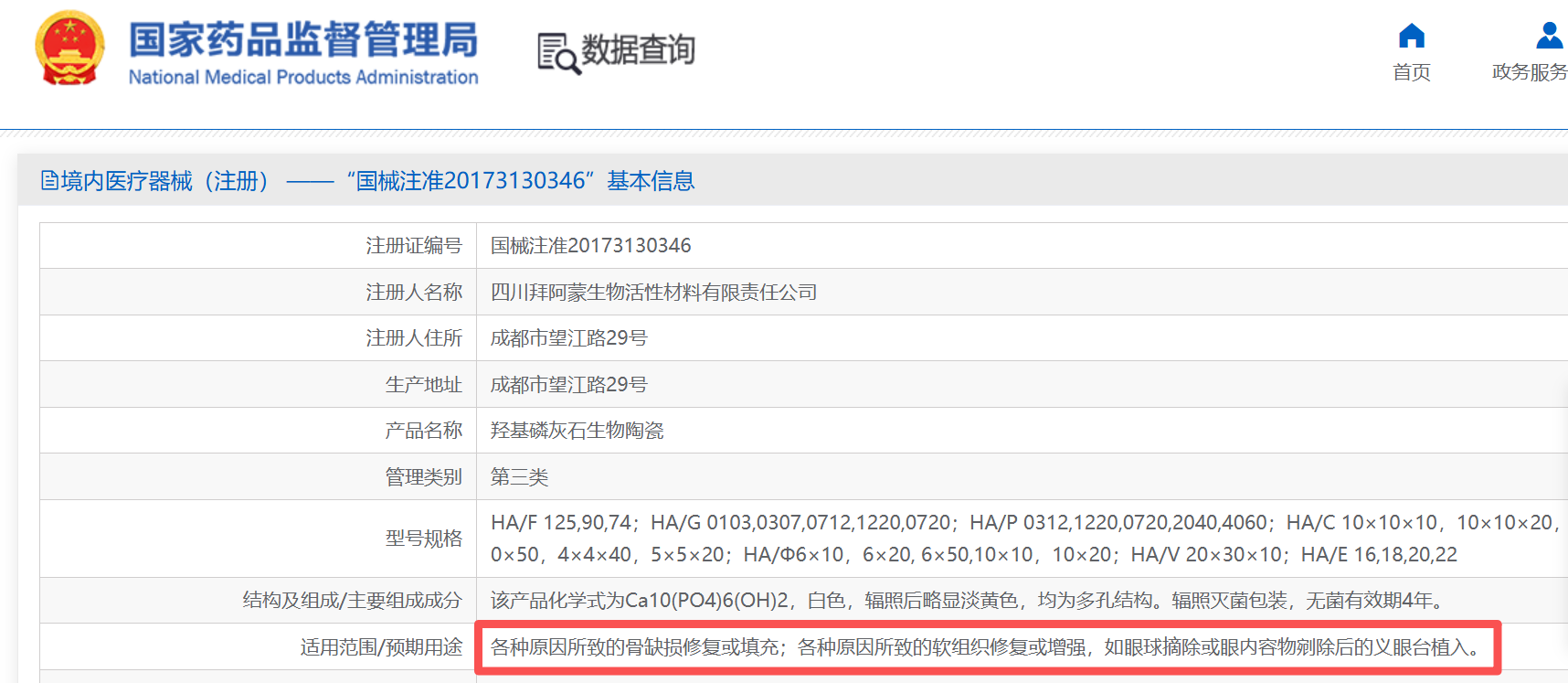
图片来源:国家药监局官网
目前,上城区卫生监督所已对杭州思达芮医疗美容诊所立案调查。而这背后,“菲林普利”是否构成“超适应证”使用?羟基磷灰石类材料在医美领域的类似应用是否存在普遍性?随着医美市场合规产品逐步扩容,如何规范此类材料的临床使用、遏制违规乱象?这些问题已成为亟待破解的行业课题。
超适应症使用?
作为一种与人体骨骼、牙齿无机成分高度相似的材料,羟基磷灰石凭借优良的生物相容性,既可用于骨缺损填充、牙齿脱敏美白等场景,也被引入医美领域用于面部填充来改善轮廓,像隆鼻、隆下颏等。和传统填充材料相比,其效果更持久,但也可能存在局部炎症反应等情况。
21世纪经济报道记者以“羟基磷灰石”为关键词,在药品监督管理局共查询到175条注册信息,适用范围多集中于骨科、口腔等治疗领域,包括“羟基磷灰石涂层人工髋关节”“羟基磷灰石义眼台”“骨修复材料”“髋关节假体”“口腔用骨修复材料”等。
但在医美市场中,菲林普利、海魅云境、悦龄塑等羟基磷灰石类产品已为求美者所熟知。国家药监局备案信息显示,上海睿星医疗器材有限公司注册的悦龄塑(复合磷酸钙骨植入材料)、上海倍尔康生物医学科技有限公司注册的海魅云境(羟基磷灰石生物陶瓷),适用范围均为“非承重性骨缺损的填充”。
信达证券2024年初发布的研报显示,悦龄塑推出三种规格适用于不同层位/部位的抗衰;2021年上市的菲林普利以L/M/S型的微球粒径依次从大到小,注射层位由深至浅,分别为皮下深层、真皮深层、真皮层;2023年上市的海魅云境主打“5G记忆型再生填充”。
市场宣传与实际应用或已突破注册限制。“国内的部分已上市产品的适应证,不完全与当前医美机构治疗使用场景中消费者实际需求匹配,因而从合规宣传角度存在一定风险。”信达证券研报同时提示风险。
如何界定“超适应证”?联合丽格医疗美容集团创始人、董事长李滨此前在接受21世纪经济报道记者采访时解释,根据国家药监局的产品注册证信息,“羟基磷灰石生物陶瓷”的适用范围为“适用于非承重性骨缺损的填充”。从这一适用范围来看,医生只要贴着骨膜注射这一产品,用于非承重性骨缺损的修复,或者是跟骨缺损相关联的注射填充,那就是在适应证之内。同时要注意,要用于“非承重骨”,例如腿骨就不能注射,因为有承重作用,但面部就属于非承重骨。
但对于部分适应证明确用于口腔或者骨科的产品,李滨认为,这些产品本身是安全的,只不过适应证在于别的部位,打在面部可能属于超适应证。
也有资深医美业内人士向21世纪经济报道记者表示,我国目前尚无针对医疗器械超适应证使用的明确法律条文,实践中多参考《中华人民共和国医师法》中关于药品超适应证使用的规定,即在无有效或更好治疗手段等特殊情况下,医师取得患者明确知情同意后,可采用有循证医学证据的未明确用法。
“病历管理是核心风险控制点。”该人士补充,规范的病历书写能完整留存患者知情同意证明,在当前法律依据不足的背景下,这已成为行业内降低合规风险的主要实践方式。
合规产品落地
尽管羟基磷灰石在医美领域的“超适应证”使用乱象引发争议,但这一材料的市场潜力仍获行业普遍看好。信达证券研报援引ASPS(美国整形外科协会)数据指出,海外市场中羟基磷灰石疗程数占比较低但具备更强增长动力。
作为国际医美领域三大再生材料之一,羟基磷灰石与聚左旋乳酸 PLLA(童颜针主要成分)、聚己内酯 PLC(少女针主要成分)齐名。市场期待之下,2025年国内羟基磷灰石医美产品迎来密集获批,为行业规范化发展带来新契机。
今年2月,摩漾生物科技有限公司旗下产品Aphranel®优法兰(注射用羟基磷酸钙微球面部填充剂)正式获得国家药品监督管理局批准的三类医疗器械注册认证,用于鼻唇沟部位皮下层注射,以纠正中重度鼻唇沟皱纹。
作为中国首个获批用于面部软组织填充的羟基磷酸钙注射针剂,优法兰在公众号中强调,“这一里程碑式的突破不仅彰显了摩漾生物在生物材料领域的卓越造诣,更开启了中国医疗美容行业CaHA领域的规范化新纪元。”
仅一个月后,Merz North America Inc.(梅尔茨北美公司)的注射用羟基磷酸钙微球面部填充剂Radiesse(“瑞德喜”)获国家药监局批准,用于注射到鼻唇沟部位皮下层,以纠正中重度鼻唇沟皱纹。
瑞德喜由此也成为国内首个获批的进口羟基磷灰石面部注射剂,也是国内第二款获批的羟基磷灰石面部注射产品。同时,该产品也是唯一一款经美国食品药品监督管理局(FDA)批准的羟基磷灰石医美注射剂。
但合规产品的陆续落地,似乎并未完全根治“超适应证”使用的行业沉疴。“当前医美行业存在诸多乱象,其中超适应证使用医美产品的问题尤为突出。”前述资深医美业内人士指出,几乎所有注射类医美产品都存在超适应证使用的情况,“以羟基磷酸钙为例,摩漾和Merz获批的适应证同样是鼻唇沟,然而在面部其他部位进行注射的现象屡见不鲜,这显然也属于超适应证使用。”
而在市场需求与合规要求的双重驱动下,不少企业也加速布局羟基磷灰石赛道。例如昊海生科在2025年半年报中披露,公司在研管线包含“注射用羟基磷灰石微球组织填充剂”,该产品采用无颗粒交联透明质酸钠凝胶作为赋形剂,该赋形剂优异的内聚性以及独特的微观结构促使羟基磷灰石均匀有序地分布,具有即时填充的效果,同时均匀有序地分布可以有效调节胶原生成速度和质量,减少不良反应的发生,安全性更高。
全链条监管加码
随着更多合规羟基磷灰石产品获批上市,行业规范化发展的基础不断夯实。多位业内人士向记者表示,多数正规医美机构在医生职业道德约束与严格监管双重作用下,能够遵守产品使用规范,但部分具备欺诈属性的机构仍存在违规操作,成为行业治理的重点难点。
“医美行业仍存在无资质机构开展诊疗、使用不合规产品等问题,监管面临多重挑战。”前述资深业内人士举例称,部分生活美容院私下开展医美项目,甚至有从业者在酒店房间等非合规场所为消费者注射,这类隐蔽性违规行为大幅增加了监管难度,“近年来监管力度持续加大,行业整体合规水平较以往已有明显提升,但彻底根治乱象仍需长期努力。”
人民群众“美丽消费”需求的升级,推动医美行业监管体系不断完善。今年以来,多地多部门密集出台监管政策、开展专项整治,从资质管理、产品流通到服务规范等全链条筑牢行业防线。
例如今年5月,青海省海南州卫生健康委员会启动为期7个月的非法医疗美容专项整治行动,重点打击非法从事医疗美容诊疗活动;使用无资质人员开展双眼皮、纹绣、线雕等项目;违法发布医疗美容广告;违法采购、使用医疗美容类药品和医疗器械,违法违规经营使用注射用透明质酸钠、胶原蛋白、肉毒素等行为。
9月,福建省泉州市市场监管局与泉州市卫生健康委联合印发《泉州市生活美容与医疗美容行业合规指引》,从资质管理、广告宣传、产品使用、消费者权益保护等多维度,为美业经营划定“红线”与“底线”,推动行业健康发展。
11月14日,济宁市任城区四部门联合启动医美市场专项执法行动,以“全覆盖排查、全链条打击、长效化治理”为目标,重点整治四大类突出问题,包括严查无证行医行为、严打药械非法流通、整治市场经营乱象、清理网络不良信息。资料显示,该行动已排查各类医美相关场所50余家,现场查封医疗美容设备10余台,下达责令整改通知书8份。
国家层面的监管改革也在同步推进,且监管逻辑从医美注射类等医疗器械延伸至整个“美丽消费”领域。11月17日,国家药监局发布《关于深化化妆品监管改革促进产业高质量发展的意见》,目标到2030年,我国化妆品监管法律制度更加完善,标准体系更加健全,技术支撑更加有力,产业创新活力更加充沛,风险防控能力全面加强,质量安全水平显著提升。
事实上,包括羟基磷灰石在内的医美产品规范化发展,既需企业加速合规产品研发,更要监管部门构建全链条机制,唯有多方合力,才能让医美行业在安全轨道上实现高质量发展。


